LLNL, BridgeBio开始试验新的超级计算抗癌药物
Lawrence Livermore国家实验室(LLNL)和BridgeBio肿瘤学治疗公司(BridgeBio)今天宣布,一种针对多种癌症中涉及的特定基因突变的药物的临床试验已经开始,这是超级计算辅助药物设计的一个重要里程碑。
新药BBO-8520的开发是LLNL、BridgeBio和美国国家癌症研究所(NCI)弗雷德里克国家癌症研究实验室(FNL) RAS倡议合作的结果。这是美国能源部(DOE)国家实验室首次通过DOE在任务应用高性能计算(HPC)方面的领导地位,结合llnl开发的集成人工智能(AI)和传统物理药物发现的平台,以及与FNL和NCI的有效合作伙伴关系,发现了这种药物。
这种候选药物在实验室测试中显示出抑制与约30%的癌症相关的KRAS蛋白突变的希望——长期以来被癌症研究人员认为是“不可药物”的目标。这一成果为肿瘤中含有易感KRAS突变的癌症患者提供了广泛影响的希望。这表明,计算/人工智能药物设计方法可以为癌症和癌症治疗的未来提供新的见解。
LLNL生物化学和生物物理系统小组组长Felice Lightstone说:“对于美国能源部来说,这是高性能计算可以加速药物发现的第一个真正的例子,通过进行人体试验,这一点得到了加强。“通过FDA的批准进入人体试验已经表明FDA已经看过了设计,我们已经满足了实际应用的所有标准。不仅如此,我们正在把我们在高性能计算方面的基础研究转化为工业上有用的应用——这是一个真正的里程碑。”
Revolutio
通过超级计算机辅助药物发现来实现癌症治疗
经过短短三年的开发,得益于小分子研究的科学专业知识,LLNL无与伦比的HPC能力和利弗莫尔计算机辅助药物发现(LCADD)平台,美国食品和药物管理局(FDA)于2023年12月批准了BBO-8520进行人体试验。该试验将重点关注KRASG12C突变型非小细胞肺癌患者,并将测试这种新型抑制剂的安全性和有效性。
该里程碑利用了计算药物设计能力,最初是由美国能源部和nci在癌症登月计划下的长期合作伙伴关系所激发的,该伙伴关系旨在应用LLNL和其他美国能源部国家实验室的世界级计算资源,以推进癌症研究和治疗,造福公众。该项目的研究人员说,合作伙伴关系在开发一种切实可行的候选药物方面的成功,突显了联合美国能源部国家实验室、生物医学研究机构和创新公司的专业知识来解决癌症等困难挑战的价值。它还表明,与传统的药物发现过程相比,计算方法可以节省数百万美元和宝贵的时间——可能是数年——在传统的药物发现过程中,即使是有希望的化合物也可能在进入人体测试之前失败。
“通过与LLNL和FNL的合作,我们在抑制导致癌症的KRAS突变的药物发现方面取得了重大成就,”BridgeBio肿瘤学治疗公司首席科学官Pedro Beltran说。“BBO-8520的开发只有通过我们的合作方式才能实现,这体现了团队合作和创新的力量。这种药物能够在创纪录的时间内进入人体试验,体现了计算和人工智能药物设计的潜力,可以节省新药发现的时间、金钱和实验室资源。这证明了我们合作的光明前景,也证明了它可以给有需要的患者带来希望。我们很自豪能继续与LLNL和FNL合作,推动癌症研究的发展。”
除了推进癌症研究,LLNL的代表表示,这一里程碑验证了将超级计算与人工智能和基于物理的计算平台相结合,有可能进一步加速小分子药物的发现,并使能源部、国家核安全局和LLNL有能力快速、常规地开发针对疾病或未来流行病的医疗对策,与生物安全领域更广泛的任务重点领域保持一致。生物弹性和国家安全。
LLNL的科学技术副主任Pat Falcone说:“通过这种开创性的合作,LLNL、弗雷德里克国家癌症研究实验室和BridgeBio已经在与癌症的斗争中开启了乐观的灯塔——这只是我们希望长期而富有成效的合作的开始。”“这种药物从计算模拟到人体试验的快速旅程反映了美国能源部国家实验室研究的变革力量,并确保我们为下一次大流行做好更好的准备。这一合作证明了公私伙伴关系的潜力,我们邀请其他机构和公司加入我们,通过计算和人工智能辅助药物设计寻求创新解决方案。我们一起加快了发现的步伐。”
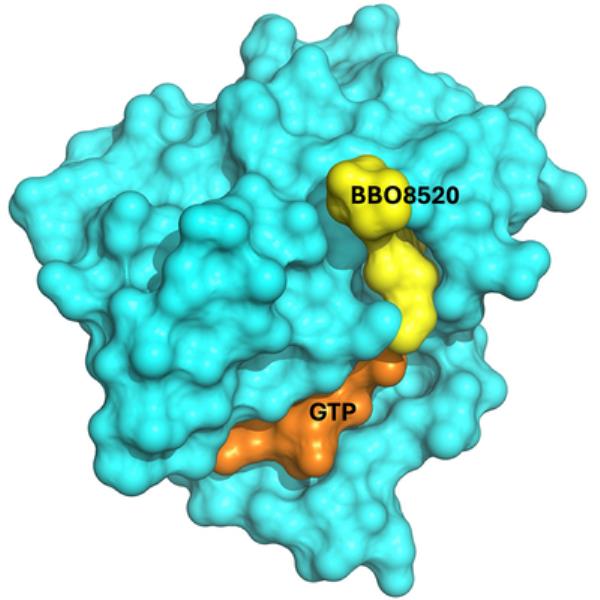
这张图片描绘了抗癌候选药物BBO-8520(黄色)、天然底物鸟苷三磷酸(或GTP,橙色)和KRAS蛋白(青色)之间相互作用的表面表示。图片由LLNL团队提供。
这项工作的最初研究和资金来自于由NCI建立的RAS倡议,该倡议旨在探索攻击由RAS基因突变形式编码的蛋白质的新方法,并最终为RAS相关癌症创造有效的新疗法。研究人员说,在所有形式的RAS蛋白中,KRAS是最理想的治疗靶点,因为突变(致癌)KRAS在胰腺癌、肺癌和结直肠癌中普遍存在。RAS基因家族的突变与20% - 30%的癌症有关,包括95%的胰腺癌和45%的结直肠癌。
“弗雷德里克国家实验室通过nci和能源部的合作,与劳伦斯利弗莫尔的同事建立了长期的合作关系,为与BridgeBio的公私合作奠定了基础,这代表了一种独特的药物开发模式,包含了世界级的计算能力,”癌症生物学家、FNL RAS倡议团队负责人德怀特·尼斯利说。“通过利用每个合作伙伴的独特优势,我们实现了NCI的长期目标,即为ras驱动的癌症开发新的治疗方案。”
正常情况下,RAS蛋白接受并跟随信号在活性和非活性状态之间切换。像电灯开关一样,KRASG12C等突变的RAS蛋白会陷入“永远开着”的状态,导致细胞生长失控;形成肿瘤和癌症扩散到身体的其他部位。虽然现有的药物治疗旨在关闭这一开关,但癌细胞有时仍会找到重新打开它的方法——随着时间的推移,治疗效果会降低。与目前大多数KRASG12C药物不同,BBO-8520靶向活性和非活性状态的KRASG12C,有效阻断其功能并阻碍癌症进展。这种双重机制被认为比现有的治疗方法更有优势,因为它解决了一些可能随着时间推移而产生的耐药性机制。
临床前研究证明了boo -8520的良好结果,在各种癌症模型中显示出统计学上显著的肿瘤生长抑制作用,即使在针对同一蛋白质的其他药物出现耐药性的情况下也是如此。领导FNL对BBO-8520临床前研究的癌症生化学家安娜·马西格(Anna Maciag)说,由于只与“off”构象结合,现有的治疗方法“导致患者很快产生耐药性”,从而导致癌症进展。Maciag补充说:“这种双重抑制剂同时达到‘开’和‘关’状态,可以100%覆盖靶标。”
这些研究表明,BBO-8520在治疗某些类型的癌症方面具有更有效的潜力,特别是那些由KRASG12C基因突变驱动的癌症,KRASG12C基因在癌细胞生长和增殖中起着关键作用,几十年来一直被科学界认为是不可药物的。
虽然一个典型的药物发现项目需要合成数千种有前途的化合物来设计和开发一种药物,但这项研究背后的团队最初只合成了几百种化合物来发现boo -8520——使用基于人工智能和物理的LCADD平台来缩小可能成功合成的小分子的数量。利用数千种化合物的硅模型,该团队为整个项目合成了大约850种化合物。
此次合作源于LLNL和BridgeBio oncology Therapeutics以及BridgeBio和FNL之间的合作研究与开发协议(crada),旨在推进新型RAS抑制剂治疗癌症的发现。crada将这三家机构联合起来,共同应对癌症治疗中最具挑战性的方面:将药物推向市场的漫长时间以及有希望的候选药物的高失败率。LLNL还将这个问题视为高级计算的一个重要用例。在未来几年,LLNL和BridgeBio将继续为RAS计划确定的其他靶点寻找新的化合物,实验测试和验证这些化合物,分析化合物与靶点之间的相互作用,并优化现有化合物。
LLNL的计算化学家和该项目的首席研究员岳阳说:“这是一个具有共同愿景的真正合作精神的典型例子:开发精确有效的针对ras驱动癌症的创新疗法,为癌症患者带来新的希望。”“我们要感谢BridgeBio信任我们成为他们团队的一员,并对未来的候选人以及他们正在进行的药物发现工作产生影响。BridgeBio愿意将我们纳入他们的计划是这种药物成功的关键。”
Yang补充说,用于发现BBO-8520的LCADD平台是广泛的,可定制用于多种疾病,包括其他形式的癌症和传染病。通过与美国工业界合作,科学家可以测试和改进该平台,以确保有效的系统对抗未来的生物威胁。
LLNL创新与合作办公室(IPO)业务发展主管Yash Vaishnav与BridgeBio子公司Theras就CRADA进行了谈判,并与BridgeBio oncology Therapeutics就该候选药物的许可协议进行了谈判。Vaishnav还管理根据CRADA开发的KRAS抑制剂的知识产权组合以及与BridgeBio同行的关系。IPO是LLNL与行业接触的焦点,旨在通过确定新的经济机会和解决方案,并通过许可或合作伙伴关系将其转移到私营部门,从而加速美国的竞争力。